O degelo rápido do permafrost no Ártico tem o potencial de liberar bactérias resistentes a antibióticos, vírus não descobertos e até mesmo resíduos radioativos de reatores nucleares e submarinos
Pela Agência Espacial Europeia*
Ao considerar as implicações do degelo do permafrost, nossas preocupações iniciais provavelmente se voltarão para a grande questão do metano sendo liberado na atmosfera e exacerbando o aquecimento global ou problemas para as comunidades locais conforme o solo e a infraestrutura se tornam instáveis. Embora isso seja ruim o suficiente, uma nova pesquisa revela que os efeitos potenciais do degelo do permafrost também podem representar sérias ameaças à saúde.
Como parte do Arctic Methane and Permafrost Challenge da ESA – NASA , uma nova pesquisa revelou que o degelo rápido do permafrost no Ártico tem o potencial de liberar bactérias resistentes a antibióticos, vírus não descobertos e até mesmo resíduos radioativos de reatores nucleares e submarinos da Guerra Fria.
O permafrost, ou terra permanentemente congelada, cobre cerca de 23 milhões de quilômetros quadrados no hemisfério norte. A maior parte do permafrost no Ártico tem até um milhão de anos – normalmente, quanto mais profundo, mais antigo.
Além de micróbios, ele abrigou uma ampla gama de compostos químicos ao longo de milênios, seja por meio de processos naturais, acidentes ou armazenamento deliberado. No entanto, com a mudança climática fazendo com que o Ártico aqueça muito mais rápido do que o resto do mundo, estima-se que até dois terços do permafrost próximo à superfície pode ser perdido até 2100.
O degelo do permafrost libera gases de efeito estufa – dióxido de carbono e metano – para a atmosfera, além de causar mudanças abruptas na paisagem.
No entanto, uma pesquisa , publicada recentemente na Nature Climate Change , descobriu que as implicações do declínio do permafrost poderiam ser muito mais difundidas – com potencial para a liberação de bactérias, vírus desconhecidos, lixo nuclear e radiação e outros produtos químicos preocupantes.
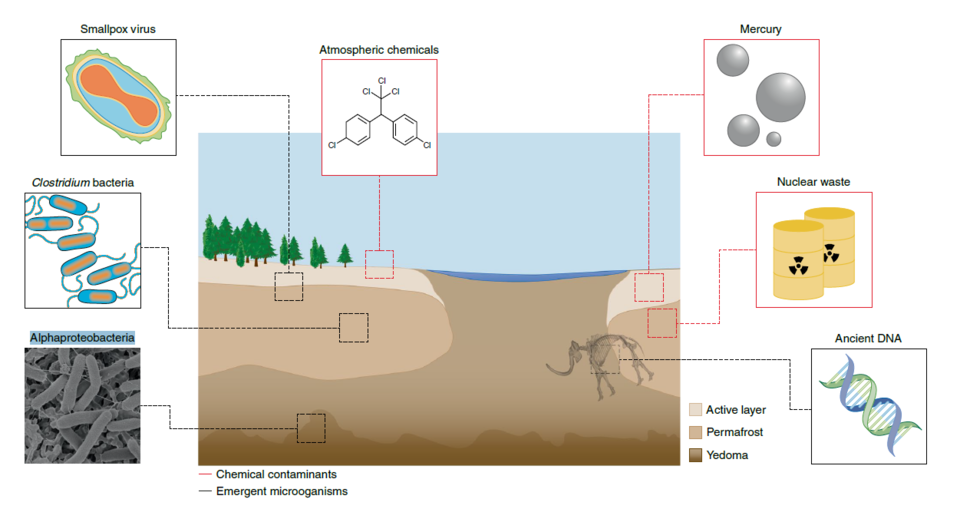
Armazenamento de riscos no permafrost ártico
O artigo descreve como o permafrost profundo, a uma profundidade de mais de três metros, é um dos poucos ambientes na Terra que não foi exposto aos antibióticos modernos. Mais de 100 microrganismos diversos no permafrost profundo da Sibéria foram considerados resistentes a antibióticos. Conforme o permafrost descongela, há potencial para que essas bactérias se misturem com a água do degelo e criem novas cepas resistentes a antibióticos.
Outro risco diz respeito aos subprodutos de combustíveis fósseis, que foram introduzidos em ambientes permafrost desde o início da revolução industrial. O Ártico também contém depósitos de metais naturais, incluindo arsênio, mercúrio e níquel, que foram extraídos por décadas e causaram grande contaminação de resíduos em dezenas de milhões de hectares.
Poluentes e produtos químicos agora banidos, como o inseticida dicloro-difenil-tricloroetano, DDT, que foram transportados para o Ártico atmosférico e com o tempo ficaram presos no permafrost, correm o risco de permear novamente a atmosfera.
Além disso, o aumento do fluxo de água significa que os poluentes podem se dispersar amplamente, danificando espécies de animais e pássaros, bem como entrando na cadeia alimentar humana.
Há também maior possibilidade de transporte de poluentes, bactérias e vírus. Mais de 1000 assentamentos, sejam de extração de recursos, projetos militares e científicos, foram criados em permafrost durante os últimos 70 anos. Isso, junto com a população local, aumenta a probabilidade de contato ou liberação acidental. Apesar das descobertas da pesquisa, ele diz que os riscos de microrganismos emergentes e produtos químicos dentro do permafrost são mal compreendidos e em grande parte não quantificados. Afirma que uma investigação mais aprofundada na área é vital para obter uma melhor compreensão dos riscos e para desenvolver estratégias de mitigação.
O autor principal da revisão, Kimberley Miner, do Laboratório de Propulsão a Jato da NASA, disse: “Temos uma compreensão muito pequena de que tipo de extremófilos – micróbios que vivem em muitas condições diferentes por um longo tempo – têm o potencial de ressurgir. Esses são micróbios que co-evoluíram com coisas como preguiças gigantes ou mamutes, e não temos ideia do que eles poderiam fazer quando liberados em nossos ecossistemas.
“É importante entender os impactos secundários e terciários dessas mudanças em grande escala da Terra, como o degelo do permafrost. Embora alguns dos riscos associados ao degelo de até um milhão de anos de material tenham sido capturados, estamos muito longe de sermos capazes de modelar e prever exatamente quando e onde eles acontecerão. Esta pesquisa é crítica. ”
Diego Fernandez, da ESA, acrescentou: “A pesquisa conduzida como parte do Desafio de Metano Ártico e Permafrost da ESA – NASA no âmbito do nosso programa Ciência para a Sociedade é vital para compreender a ciência do Ártico em mutação. O descongelamento do permafrost claramente apresenta enormes desafios, mas são necessárias mais pesquisas. A NASA e a ESA estão unindo forças para promover a colaboração científica em todo o Atlântico para garantir o desenvolvimento de ciência e conhecimento sólidos para que os tomadores de decisão estejam armados com as informações corretas para ajudar a resolver esses problemas. ”
Referência:
Miner, K.R., D’Andrilli, J., Mackelprang, R. et al. Emergent biogeochemical risks from Arctic permafrost degradation. Nat. Clim. Chang. 11, 809–819 (2021). https://doi.org/10.1038/s41558-021-01162-y
Henrique Cortez *, tradução e edição.
in EcoDebate, ISSN 2446-9394, 26/10/2021
Autor: Henrique Cortez
Fonte: EcoDebate
Sítio Online da Publicação: EcoDebate
Data: 26/10/2021
Publicação Original: https://www.ecodebate.com.br/2021/10/26/degelo-do-permafrost-pode-liberar-bacterias-e-virus/




 Laboratório Phenotypic Screening Platform foi reformado por meio de uma parceria com a empresa Eurofarma – Foto: Cecília Bastos/USP Imagens
Laboratório Phenotypic Screening Platform foi reformado por meio de uma parceria com a empresa Eurofarma – Foto: Cecília Bastos/USP Imagens Grupo de pesquisa Phenotypic Screening Platform, do ICB, onde são realizadas as análises de triagem fenotípica – Foto: Cecília Bastos/USP Imagens
Grupo de pesquisa Phenotypic Screening Platform, do ICB, onde são realizadas as análises de triagem fenotípica – Foto: Cecília Bastos/USP Imagens Placa de ensaio com os 384 poços para analisar a reação de compostos ao vírus da febre amarela – Foto: Cecília Bastos/USP Imagens
Placa de ensaio com os 384 poços para analisar a reação de compostos ao vírus da febre amarela – Foto: Cecília Bastos/USP Imagens
/s.glbimg.com/jo/g1/f/original/2015/05/25/virus-ebola.jpg)
/i.s3.glbimg.com/v1/AUTH_59edd422c0c84a879bd37670ae4f538a/internal_photos/bs/2018/T/s/AAhRiGQ5KAdu1WGmYEMw/ebola.jpg)



/i.s3.glbimg.com/v1/AUTH_59edd422c0c84a879bd37670ae4f538a/internal_photos/bs/2018/O/u/TbYHvRSCyUd1p0itA61A/frame-00-00-03.440.jpg)